Tikrit Medical College, Urology, Fifth year
1
أ.د. حممد حمسن عبد العزيز
Urinary Stones
Kidney stones: epidemiology
~10% of Caucasian men will develop a kidney stone by the age of 70.
Within 1 year of a calcium oxalate stone, 10% of men will form another calcium
oxalate stone, and 50% will have formed another stone within 10 years. The
prevalence of renal tract stone disease is determined by factors intrinsic to
the individual and by extrinsic (environmental) factors. A combination of
factors often contributes to risk of stone formation.
Intrinsic factors
Age. The peak incidence of stones occurs between the ages of 20-50
years.
Sex. Males are affected 3 times as frequently as females.
Genetic. ~25% of patients with kidney stones report a family history of
stone disease.
Extrinsic (environmental) factors
Geographical location, climate, and season.
Ureteric stones become more prevalent during the summer, the highest
incidence occurring a month or so after peak summertime temperatures,
presumably because of higher urinary concentration in the summer
(encourages crystallization). Concentrated urine has a lower pH,
encouraging cystine and uric acid stone formation. Exposure to sunlight
may also increase endogenous vitamin D production, leading to
hypercalciuria.
Water intake. Low fluid intake (<1200ml/day) predisposes to stone
formation.
Diet. High animal protein intake increases risk of stone disease (high
urinary oxalate, low pH, low urinary citrate). High salt intake causes
hypercalciuria. Contrary to conventional teaching, low calcium diets
predispose to calcium stone disease, and high calcium intake is protective.
Occupation. Sedentary occupations predispose to stones compared with
manual workers.
Kidney stones: types and predisposing factors
Stones may be classified according to composition, X-ray appearance, or size
and shape.
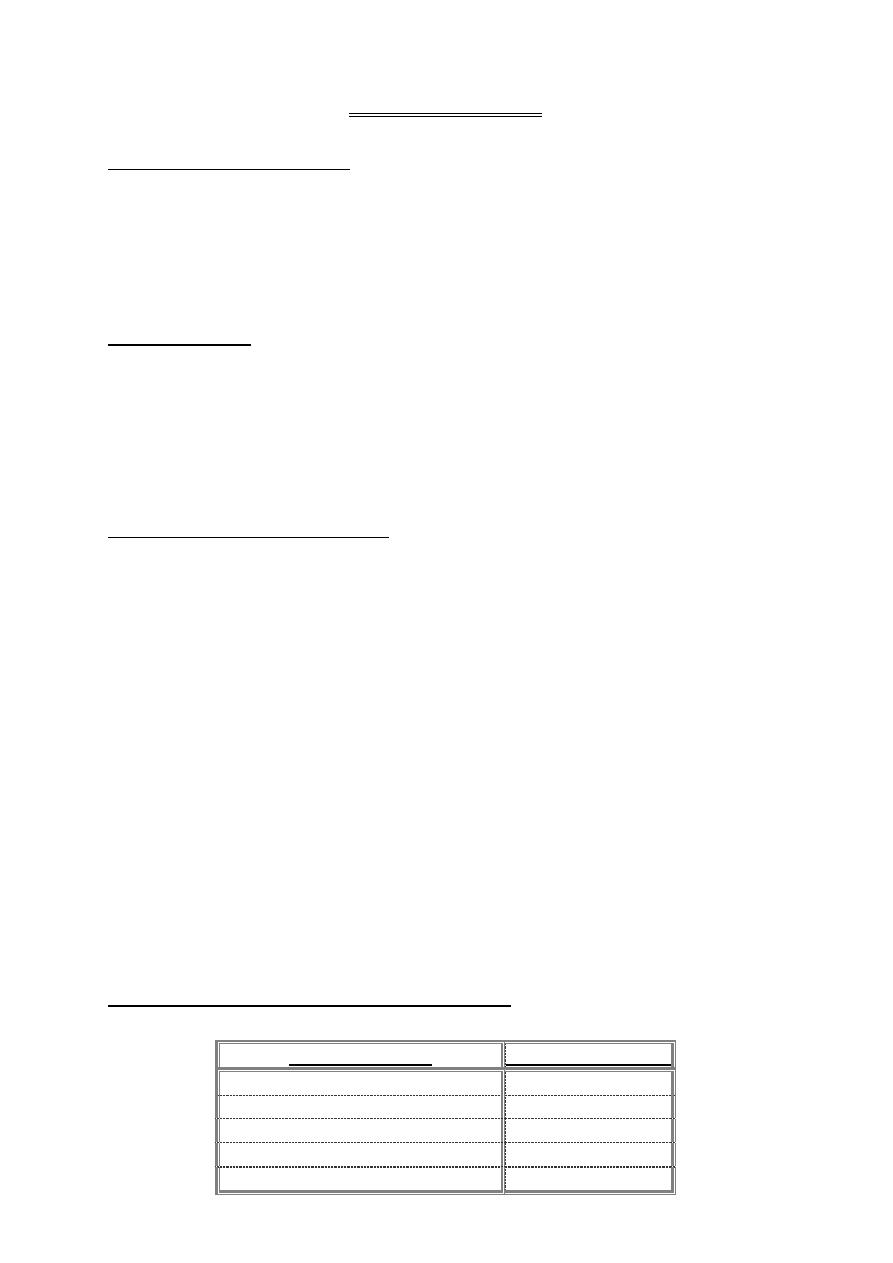
Stone composition
% of all renal calculi
Calcium oxalate
85%
Uric acid
5-10%
Calcium phosphate + calcium oxalate
10%
Struvite (infection stones)
2-20%
Cystine
1%

Tikrit Medical College, Urology, Fifth year
2
أ.د. حممد حمسن عبد العزيز
Other rare stone types (all of which are radiolucent): indinavir
(a protease inhibitor used for treatment of HIV); triamterene (a relatively
insoluble potassium sparing diuretic, most of which is excreted in urine);
xanthine.
Radiodensity on X-ray
Radio-opaque
Opacity implies the presence of substantial amounts of calcium within the
stone. Calcium phosphate stones are the most radiodense stones, being almost
as dense as bone. Calcium oxalate stones are slightly less radiodense.
Relatively radiodense
Cystine stones are relatively radiodense because they contain sulphur.
Magnesium ammonium phosphate (struvite) stones are less radiodense than
calcium containing stones.
Completely radiolucent
Uric acid, triamterene, xanthine, (indinavir cannot be seen even on CTU).
Size and shape
Stones can be characterized by their size, in centimeters. Stones which
grow to occupy the renal collecting system (the pelvis and one or more renal
calyx) are known as staghorn calculi, since they resemble the horns of a stag.
They are most commonly composed of struvite (magnesium ammonium
phosphate)(being caused by infection and forming under the alkaline conditions
induced by urea-splitting bacteria), but may be composed of uric acid, cystine,
or calcium oxalate monohydrate.
Kidney stones: mechanisms of formation
Periods of intermittent supersaturation of urine with various substances
can occur as a consequence of dehydration and following meals. The earliest
phase of crystal formation is known as nucleation. Crystal nuclei usually form on
the surfaces of epithelial cells or on other crystals. Crystal nuclei form into
clumps: a process known as aggregation. Citrate and magnesium not only inhibit
crystallization but also inhibit aggregation.
Factors predisposing to specific stone types
Calcium oxalate (~85% of stones)
Hypercalciuria
Hypercalcaemia: Almost all patients with hypercalcaemia who form stones
have primary hyperparathyroidism.
Hyperoxaluria
Hypocitraturia: Low urinary citrate excretion. Citrate forms a soluble
complex with calcium, so preventing complexing of calcium with oxalate to
form calcium oxalate stones.
Hyperuricosuria: High urinary uric acid levels

Tikrit Medical College, Urology, Fifth year
3
أ.د. حممد حمسن عبد العزيز
Uric acid (~5-10% of stones)
Gout: 50% of patients with uric acid stones have gout.
Myeloproliferative disorders. Particularly following treatment with
cytotoxic drugs.
Idiopathic uric acid stones (no associated condition).
Calcium phosphate (calcium phosphate + calcium oxalate = 10% of stones)
Occur in patients with distal renal tubular acidosis (RTA)
Struvite (infection or triple phosphate stones) (2-20% of stones)
These stones are composed of magnesium, ammonium, and phosphate.
They form as a consequence of urease-producing bacteria which produce
ammonia from breakdown of urea. Under alkaline conditions, crystals of
magnesium, ammonium, and phosphate precipitate.
Cystine (1% of all stones)
Occur only in patients with cystinuria: an inherited (autosomal-recessive)
disorder
Evaluation of the stone former
Determination of stone type and a metabolic evaluation allows
identification of the factors that led to stone formation, so advice can be given
to prevent future stone formation. Stone type is analyzed by polarizing
microscopy, X-ray diffraction, and infrared spectroscopy, rather than by
chemical analysis. Where no stone is retrieved, its nature must be inferred
from its radiological appearance (e.g. a completely radiolucent stone is likely to
be composed of uric acid) or from more detailed metabolic evaluation.
Risk factors for stone disease
Diet. Enquire about volume of fluid intake, meat consumption (causes
hypercalciuria, high uric acid levels, low urine pH, low urinary citrate),
multivitamins (vitamin D increases intestinal calcium absorption), high
doses of vitamin C (ascorbic acid causes hyperoxaluria).
Drugs. Corticosteroids (increase enteric absorption of calcium, leading to
hypercalciuria); chemotherapeutic agents (breakdown products of
malignant cells leads to hyperuricaemia).
Urinary tract infection. Urease-producing bacteria (Proteus, Klebsiella,
Serratia, Enterobacter) predispose to struvite stones.
Mobility. Low activity levels predispose to bone demineralization and
hypercalciuria.
Systemic disease. Gout, primary hyperparathyroidism, sarcoidosis.

Tikrit Medical College, Urology, Fifth year
4
أ.د. حممد حمسن عبد العزيز
Family history. Cystinuria, RTA.
Renal anatomy. PUJO, horseshoe kidney.
Previous bowel resection or inflammatory bowel disease. Causes intestinal
hyperoxaluria.
Urine pH
Urine pH in normal individuals shows variation, from pH 5-7. After a meal,
pH is initially acid. This is followed by an alkaline tide, pH rising to >6.5. Urine
pH can help establish what type of stone the patient may have (if a stone is not
available for analysis), and can help the urologist and patient in determining
whether preventative measures are likely to be effective or not.
pH <6 in a patient with radiolucent stones suggests the presence of uric
acid stones.
pH consistently >5.5 suggests type 1 (distal) RTA (~70% of such patients
will form calcium phosphate stones).
Kidney stones: presentation and diagnosis
Kidney stones may present with symptoms or be found incidentally during
investigation of other problems. Presenting symptoms include pain or haematuria
(microscopic or occasionally macroscopic). Struvite staghorn calculi classically
present with recurrent UTIs. Malaise, weakness, and loss of appetite can also
occur. Less commonly, struvite stones present with infective complications
(pyonephrosis, perinephric abscess, septicaemia, xanthogranulomatous
pyelonephritis).
Diagnostic tests
Plain abdominal radiography: calculi that contain calcium are radiodense.
Sulphur-containing stones (cystine) are relatively radiodense on plain
radiography.
Radiodensity of stones in decreasing order: calcium phosphate > calcium
oxalate > struvite (magnesium ammonium phosphate) >> cystine.
Completely radiolucent stones (e.g. uric acid, triamterene, indinavir) are
usually suspected on the basis of the patient's history and/or urine pH ,
and the diagnosis may be confirmed by ultrasound, or CTU.
Renal ultrasound: its sensitivity for detecting renal calculi is ~95%.
A combination of plain abdominal radiography and renal ultrasonography is
a useful screening test for renal calculi.
IVU: increasingly being replaced by CTU. Useful for patients with
suspected indinavir stones (which are not visible on CT).

Tikrit Medical College, Urology, Fifth year
5
أ.د. حممد حمسن عبد العزيز
CTU: a very accurate method of diagnosing all but indinavir stones. Allows
accurate determination of stone size and location and good definition of
pelvicalyceal anatomy.
Kidney stone treatment options: watchful waiting
The traditional indications for intervention are pain, infection, and
obstruction. Haematuria caused by a stone is only very rarely severe or
frequent enough to be the only reason to warrant treatment.
Options for stone treatment are watchful waiting, ESWL, flexible
ureteroscopy, PCNL, open surgery, and medical dissolution therapy.
When to watch and wait and when not to?
It is not necessary to treat every kidney stone. Thus, one would be
inclined to do nothing about a 1cm symptomless stone in the kidney of
a 95-year-old patient. On the other hand, a 1cm stone in a symptomless
20-year-old runs the risk over the remaining (many) years of the patient's life
of causing problems. It could drop into the ureter causing ureteric colic, or it
could increase in size and affect kidney function or cause pain.
Asymptomatic stones which are followed over a 3-year period are more
likely to require intervention (surgery or ESWL) or to increase in size or cause
pain if they are >4mm in diameter and if they are located in a middle or lower
pole calyx.
Another factor determining the need for treatment is the patient's job.
Airline pilots are not allowed to fly if they have kidney stones, for fear that the
stones could drop into the ureter at 30,000ft, with disastrous consequences!
Some stones are definitely not suitable for watchful waiting. Untreated
struvite (i.e. infection related) staghorn calculi will eventually destroy the
kidney if untreated and are a significant risk to the patient's life. Watchful
waiting is therefore NOT recommended for staghorn calculi unless patient
comorbidity is such that surgery would be a higher risk than watchful waiting.
Historical series suggest that ~30% of patients with staghorn calculi who did
not undergo surgical removal died of renal related causes: renal failure,
urosepsis (septicaemia, pyonephrosis, perinephric abscess).
Stone fragmentation: extracorporeal shock wave lithotripsy (ESWL)
The technique of focusing externally generated shock waves at a target
(the stone). First used in humans in 1980. The first commercial lithotriptor, the
Dornier HM3, became available in 1983. ESWL revolutionized kidney and
ureteric stone treatment. X-ray, ultrasound, or a combination of both are used
to locate the stone on which the shock waves are focused. Newer lithotriptors
generate less powerful shock waves, allowing ESWL with oral or parenteral
analgesia in many cases, but they are less efficient at stone fragmentation.
Efficacy of ESWL
Likelihood of fragmention with ESWL depends on stone size and location,
anatomy of renal collecting system, degree of obesity, and stone composition.

Tikrit Medical College, Urology, Fifth year
6
أ.د. حممد حمسن عبد العزيز
Most effective for stones <2cm in diameter, in favourable anatomical locations.
Less effective for stones >2cm diameter, in lower pole stones in a calyceal
diverticulum (poor drainage), and those composed of cystine or calcium oxalate
monohydrate (very hard).
Side-effects of ESWL
ESWL causes a certain amount of structural and functional renal damage
(found more frequently the harder you look). Haematuria (microscopic,
macroscopic) and oedema are common, perirenal haematomas less so
(0.5% detected on ultrasound with modern machines, Effective renal plasma
flow (measured by renography) has been reported to fall in ~30% of treated
kidneys. There is data suggesting that ESWL may increase the likelihood of
development of hypertension. Acute renal injury may be more likely to occur in
patients with pre-existing hypertension, prolonged coagulation time, coexisting
coronary heart disease, diabetes, and in those with solitary kidneys.
Contraindications to ESWL
Absolute contraindications: pregnancy, uncorrected blood clotting disorders
(including anticoagulation).
Intracorporeal techniques of stone fragmentation (fragmentation within the
body)
Electrohydraulic lithotripsy (EHL)
Pneumatic (ballistic) lithotripsy
Ultrasonic lithotripsy
Laser lithotripsy: The holmium: YAG laser.
Kidney stone treatment: flexible ureteroscopy and laser treatment
It can also allow access to areas of the kidney where ESWL is less
efficient or where PCNL cannot reach. It is most suited to stones <2cm in
diameter. Indications for flexible ureteroscopic kidney stone treatment
ESWL failure.
Lower pole stone
Cystine stones.
Obesity such that PCNL access is technically difficult or impossible
(nephroscopes may not be long enough to reach stone).
Obesity such that ESWL is technically difficult or impossible.
Musculoskeletal deformities such that stone access by PCNL or ESWL is
difficult or impossible (e.g. kyphoscoliosis).
Stone in a calyceal diverticulum.
Bleeding diathesis where reversal of this diathesis is potentially
dangerous or difficult.
Patient preference.

Tikrit Medical College, Urology, Fifth year
7
أ.د. حممد حمسن عبد العزيز
Kidney stone treatment: percutaneous nephrolithotomy (PCNL)
PCNL is the removal of a kidney stone via a track developed between the
surface of the skin and the collecting system of the kidney. A posterior
approach is most commonly used; below the 12th rib (to avoid the pleura and far
enough away from the rib to avoid the intercostals, vessels, and nerve). The
preferred approach is through a posterior calyx, rather than into the renal
pelvis, because this avoids damage to posterior branches of the renal artery
which are closely associated with the renal pelvis. General anaesthesia is usual,
though regional or even local anaesthesia (with sedation) can be used.
Indications for PCNL
PCNL is generally recommended for stones >3cm in diameter, those that
have failed ESWL and/or an attempt at flexible ureteroscopy and laser
treatment. It is the first-line option for staghorn calculi, with ESWL and/or
repeat PCNL being used for residual stone fragments.
For stones 2-3cm in diameter, options include ESWL (with a JJ stent in
situ), flexible ureteroscopy and laser treatment, and PCNL.
Kidney stones: open stone surgery
Indications
Complex stone burden (projection of stone into multiple calyces, such
that multiple PCNL tracks would be required to gain access to all the
stone)
Failure of endoscopic treatment
Anatomic abnormality that precludes endoscopic surgery (e.g. retrorenal
colon)
Body habitus that precludes endoscopic surgery (e.g. gross obesity,
kyphoscoliosis)
Patient request for a single procedure where multiple PCNLs might be
required for stone clearance
Non-functioning kidney
Non-functioning kidney
If the kidney is non-functioning, the simplest way of removing the stone
is to remove the kidney.
Functioning kidneys options for stone removal
Small- to medium-sized stones: Pyelolithotomy, Radial nephrolithotomy.
Staghorn calculi
Anatrophic (avascular) nephrolithotomy
Extended pyelolithotomy with radial nephrotomies (small incisions over
individual stones)

Tikrit Medical College, Urology, Fifth year
8
أ.د. حممد حمسن عبد العزيز
Specific complications of open stone surgery
Wound infection (the stones operated on are often infection stones);
flank hernia; wound pain. (With PCNL these problems do not occur, blood
transfusion rate is lower, analgesic requirement is less, mobilization is more
rapid and discharge earlier; all of which account for PCNL having replaced open
surgery as the mainstay of treatment of large stones.) There is a significant
chance of stone recurrence after open stone surgery (as for any other
treatment modality) and the scar tissue that develops around the kidney will
make subsequent open stone surgery technically more difficult.
Kidney stones: medical therapy (dissolution therapy)
Uric acid and cystine stones are suitable for dissolution therapy. Calcium
within either stone type reduces the chances of successful dissolution.
Uric acid stones
Uric acid stones form in concentrated, acid urine. Dissolution therapy is
based on hydration, urine alkalinization, allopurinol, and dietary manipulation:
the aim being to reduce urinary uric acid saturation. Maintain a high fluid intake
(urine output 2-3L/day), alkalinize the urine to pH 6.5-7. In those with
hyperuricaemia, add allopurinol 300mg/day. Dissolution of large stones
(even staghorn calculi) is possible with this regimen.
Cystine stones
Reduce cystine excretion (dietary restriction of the cystine precursor
amino acid methionine and also of sodium intake to <100mg/day).
Increase solubility of cystine by alkalinization of the urine to >pH 7.5,
maintenance of a high fluid intake, and use of drugs which convert cystine
to more soluble compounds.
Ureteric stones: presentation
Ureteric stones usually present with sudden onset of severe flank pain
which is colicky (waves of increasing severity are followed by a reduction in
severity, but it seldom goes away completely). It may radiate to the groin as the
stone passes into the lower ureter. Examination
Spend a few seconds looking at the patient. Ureteric stone pain is colicky
the patient moves around, trying to find a comfortable position. Patients with
conditions causing peritonitis (e.g. appendicitis, a ruptured ectopic pregnancy)
lie very still: movement and abdominal palpation are very painful. Many patients
with ureteric stones have dipstick or microscopic haematuria (and, more rarely,
macroscopic haematuria. The most important aspect of examination in a patient
with a ureteric stone confirmed on imaging is to measure their temperature. If
the patient has a stone and a fever, they may have infection proximal to the
stone. A fever in the presence of an obstructing stone is an indication for urine

Tikrit Medical College, Urology, Fifth year
9
أ.د. حممد حمسن عبد العزيز
and blood culture, intravenous fluids and antibiotics, and nephrostomy drainage
if the fever does not resolve within a matter of hours.
Ureteric stones: diagnostic radiological imaging
The intravenous urogram (IVU), for many years the mainstay of imaging in
patients with flank pain, has been replaced by CT urography (CTU). Compared
with IVU, CTU:
Has greater specificity (95%) and sensitivity (97%) for diagnosing
ureteric stones: it can identify other, non-stone causes of flank pain .
Requires no contrast administration so avoiding the chance of a contrast
reaction (risk of fatal anaphylaxis following the administration of low-
osmolality contrast media for IVU is in the order of 1 in 100,000).
Is faster, taking just a few minutes to image the kidneys and ureters. An
IVU, particularly where delayed films are required to identify a stone
causing high-grade obstruction, may take hours to identify the precise
location of the obstructing stone.
Is equivalent in cost to IVU, in hospitals where high volumes of CT scans
are done.
If you only have access to IVU, remember that it is contraindicated in
patients with a history of previous contrast reactions and should be avoided in
those with hay fever, a strong history of allergies, or asthma who have not been
pre-treated with high-dose steroids 24h before the IVU. Patients taking
metformin for diabetes should stop this for 48h prior to an IVU. Clearly, being
able to perform an alternative test, such as CTU in such patients, is very useful.
Plain abdominal X-ray and renal ultrasound are not sufficiently sensitive or
specific for their routine use for diagnosing ureteric stones.
Ureteric stones: acute management
While appropriate imaging studies are being organized, pain relief should be
given.
A non-steroidal anti-inflammatory (e.g. diclofenac) by intramuscular or
intravenous injection, by mouth or per rectum. Provides rapid and
effective pain control. Analgesic effect: partly anti-inflammatory, partly
by reducing ureteric peristalsis.
Where NSAIDS are inadequate, opiate analgesics such as pethidine or
morphine are added
There is no need to encourage the patient to drink copious amounts of
fluids nor to give them large volumes of fluids intravenously in the hope that
this will flush the stone out. Renal blood flow and urine output from the

Tikrit Medical College, Urology, Fifth year
11
أ.د. حممد حمسن عبد العزيز
affected kidney falls during an episode of acute, partial obstruction due to a
stone. Excess urine output will tend to cause a greater degree of
hydronephrosis in the affected kidney which will make ureteric peristalsis even
less efficient .
Watchful waiting
In many instances, small ureteric stones will pass spontaneously within
days or a few weeks, with analgesic supplements for exacerbations of pain.
Chances of spontaneous stone passage depend principally on stone size. Between
90-98% of stones measuring <4mm will pass spontaneously. Average time for
spontaneous stone passage for stones 4-6mm in diameter is 3 weeks. Stones
that have not passed in 2 months are unlikely to do so.
Ureteric stones: indications for intervention to relieve obstruction and/or
remove the stone
Pain which fails to respond to analgesics or recurs and cannot be
controlled with additional pain relief.
Fever. Have a low threshold for draining the kidney (usually done by
percutaneous nephrostomy).
Impaired renal function (solitary kidney obstructed by a stone, bilateral
ureteric stones, or pre-existing renal impairment which gets worse as a
consequence of a ureteric stone). Threshold for intervention is lower.
Prolonged unrelieved obstruction. This can result in long-term loss of
renal function. How long it takes for this loss of renal function to occur is
uncertain, but generally speaking the period of watchful waiting for
spontaneous stone passage tends to be limited to 4-6 weeks.
Social reasons. Young, active patients may be very keen to opt for
surgical treatment because they need to get back to work or their
childcare duties, whereas some patients will be happy to sit things out.
Airline pilots and some other professions are unable to work until they
are stone free.
Emergency temporizing and definitive treatment of the stone
Where the pain of a ureteric stone fails to respond to analgesics or
where renal function is impaired because of the stone, then temporary relief of
the obstruction can be obtained by insertion of a JJ stent or percutaneous
nephrostomy tube. Stone may pass down and out of the ureter with a stent or
nephrostomy in situ, but in many instances it simply sits where it is and
subsequent definitive treatment is still required. While JJ stents can relieve
stone pain, they can cause bothersome irritative bladder symptoms (pain in the
bladder, frequency, and urgency). JJ stents do make subsequent stone
treatment in the form of ureteroscopy technically easier by causing passive
dilatation of the ureter.

Tikrit Medical College, Urology, Fifth year
11
أ.د. حممد حمسن عبد العزيز
The patient may elect to proceed to definitive stone treatment by
immediate ureteroscopy (for stones at any location in the ureter) or ESWL
(if the stone is in the upper and lower ureter: ESWL cannot be used for stones
in the mid ureter because this region is surrounded by bone, which prevents
penetration of the shock waves).
Ureteric stone treatment
Many ureteric stones are 4mm in diameter or smaller and most such
stones (90%) will pass spontaneously, given a few weeks of watchful waiting,
with analgesics for exacerbations of pain. Average time for spontaneous stone
passage for stones 4-6mm in diameter is 3 weeks. Stones that have not passed
in 2 months are much less likely to do so, though large stones do sometimes
drop out of the ureter at the last moment.
Treatment options for ureteric stones
ESWL: in situ; after push-back into the kidney (i.e. into the renal pelvis
or calyces); or after JJ stent insertion
Ureteroscopy
PCNL
Open ureterolithotomy
Laparoscopic ureterolithotomy
The stone clearance rates for ESWL are stone-size dependent. ESWL is
more efficient for stones <1cm in diameter compared with those >1cm in size.
Conversely, the outcome of ureteroscopy is somewhat less dependent on stone
size.
Recommendations
Proximal ureteric stones
<1cm diameter: ESWL (in situ, push-back)
>1cm diameter: ESWL, ureteroscopy, PCNL
Distal ureteric stones
Both ESWL and ureteroscopy are acceptable options.
Stone free rate <1cm: 80-90% for both ESWL and ureteroscopy; >1cm:
75% for both ESWL and ureteroscopy.
Failed initial ESWL is associated with a low success rate for subsequent
ESWL. Therefore, if ESWL has no effect after 1 or 2 treatments, change
tactics.
Open ureterolithotomy and laparoscopic ureterolithotomy are used where
ESWL or ureteroscopy have been tried and failed, or were not feasible.

Tikrit Medical College, Urology, Fifth year
12
أ.د. حممد حمسن عبد العزيز
Bladder stones
Composition
Struvite (i.e. they are infection stones) or uric acid (in non-infected urine).
Adults
Bladder calculi are predominantly a disease of men aged >50 and with
bladder outlet obstruction due to BPH. They also occur in the chronically
catheterized patient (e.g. spinal cord injury patients
).
Children
Bladder stones are still common in Thailand, Indonesia, North Africa, and
the Middle East. In these endemic areas they are usually composed of
a combination of ammonium urate and calcium oxalate. A low-phosphate diet in
these areas (a diet of breast milk and polished rice or millet) results in high
peaks of ammonia excretion in the urine.
Symptoms
May be symptomless (incidental finding on KUB X-ray or bladder
ultrasound or on cystoscopy. In the neurologically intact patient: suprapubic or
perineal pain, haematuria, urgency and/or urge incontinence, recurrent UTI,
LUTS (hesitancy, poor flow).
Diagnosis
If you suspect a bladder stone, they will be visible on KUB X-ray or renal
ultrasound .
Treatment
Most stones are small enough to be removed cystoscopically (endoscopic
cystolitholapaxy), using stone-fragmenting forceps for stones that can be
engaged by the jaws of the forceps and EHL or pneumatic lithotripsy for those
that cannot. Large stones can be removed by open surgery (open
cystolithotomy).
Prevention of calcium oxalate stone formation
Low fluid intake
Low fluid intake may be the single most important risk factor for
recurrent stone formation. High fluid intake is protective, by reducing urinary
saturation of calcium, oxalate, and urate. Time to recurrent stone formation is
prolonged from 2 to 3 years in previous stone formers randomized to high fluid
vs. low fluid intake.
Dietary calcium
Conventional teaching was that high calcium intake increases the risk of
calcium oxalate stone disease. The Harvard Medical School studies have shown
that low calcium intake is, paradoxically, associated with an increased risk of
forming kidney stones, in both men and women

Tikrit Medical College, Urology, Fifth year
13
أ.د. حممد حمسن عبد العزيز
Calcium supplements
It is possible that consuming calcium supplements with a meal or with
oxalate-containing foods could reduce this small risk of inducing kidney stones.
Animal proteins
High intake of animal proteins causes increased urinary excretion of
calcium, reduced pH, high urinary uric acid, and reduced urinary citrate, all of
which predispose to stone formation.
Vegetarian diet
Vegetable proteins contain less of the amino acids phenylalanin, tyrosine,
and tryptophan that increase the endogenous production of oxalate. A
vegetarian diet may protect against the risk of stone formation.
Dietary oxalate
A small increase in urinary oxalate concentration increases calcium
oxalate supersaturation much more than does an increase in urinary calcium
concentration. Mild hyperoxaluria is one of the main factors leading to calcium
stone formation.
